Il saggio di mutagenicità in vitro
Ideato da Ames negli anni settanta, il test di Ames viene utilizzato per l’analisi della mutagenicità in una sostanza.
PRINCIPIO DEL TEST
È una mutazione all’indietro (revertante), è in vitro quindi non utilizza animali, è più veloce ed economica rispetto alla sperimentazione in vivo.
I ceppi tester di Ames S. typhimurium ed E. coli sono stati utilizzati per più di 40 anni per rilevare composti mutageni. Vengono effettuate mutazioni puntiformi nell’istidina (Salmonella typhimurium) o nell’operone del triptofano (Escherichia coli), che rendono i batteri incapaci di produrre il corrispondente amminoacido. Queste mutazioni danno luogo a organismi his- o trp che non possono crescere a meno che non vengano forniti istidina o triptofano.
Il potenziale mutageno di un campione viene valutato esponendo questi organismi che richiedono aminoacidi a concentrazioni variabili di campione e selezionando l’evento di reversione. Per selezionarel’evento di reversione vengono utilizzati terreni privi di istidina o triptofano che consentono solo a quelle cellule che hanno subito il ritorno alla prototrofia
istidina / triptofano di sopravvivere e crescere.
Un evento mutageno che causa sostituzioni di basi o mutazioni frameshift all’interno del gene può provocare un ritorno alla prototrofia degli amminoacidi. Questi batteri ripristinati cresceranno rispettivamente in terreni carenti di istidina o triptofano, mentre i batteri non ripristinati non saranno in grado di crescere. I terreni durante la fase di crescita possono essere liquidi o a base di agar.
TEST DI AMES SU PIASTRA DI AGAR OECD 471- Descrizione del test
I ceppi congelati appena scongelati vengono inoculati nel terreno di coltura e le colture vengono coltivate durante la notte a 37° C in uno agitatore di piastra in presenza (per TA98, TA100, E. coli WP2 [pKM101], E. coli WP2 uvrA [pKM101]) o assenza (per TA1535, TA1537, E. coli WP2 uvrA) di ampicillina. Le colture notturne vengono utilizzate la mattina successiva per il test di incorporazione o preincubazione di Ames.
I ceppi “tester” vengono esposti alla sostanza chimica per 20 minuti a 37 ° C prima di essere messi su piastre di agar con glucosio minimo. I componenti della miscela di preincubazione sono la miscela S9 o il tampone fosfato, la soluzione chimica in esame e la coltura batterica.
Dopo 20 min a 37°C, alla miscela viene aggiunto il top agar fuso integrato con istidina / biotina o triptofano e mantenuto a 48°C.
Il contenuto viene miscelato e versato su piastre di agar con glucosio minimo. Dopo 48-72 ore a 37°C, il numero di colonie per piastra e per dose viene contato ad occhio e confrontato con il numero di colonie spontanee revertanti ottenute nelle piastre di controllo negativo.
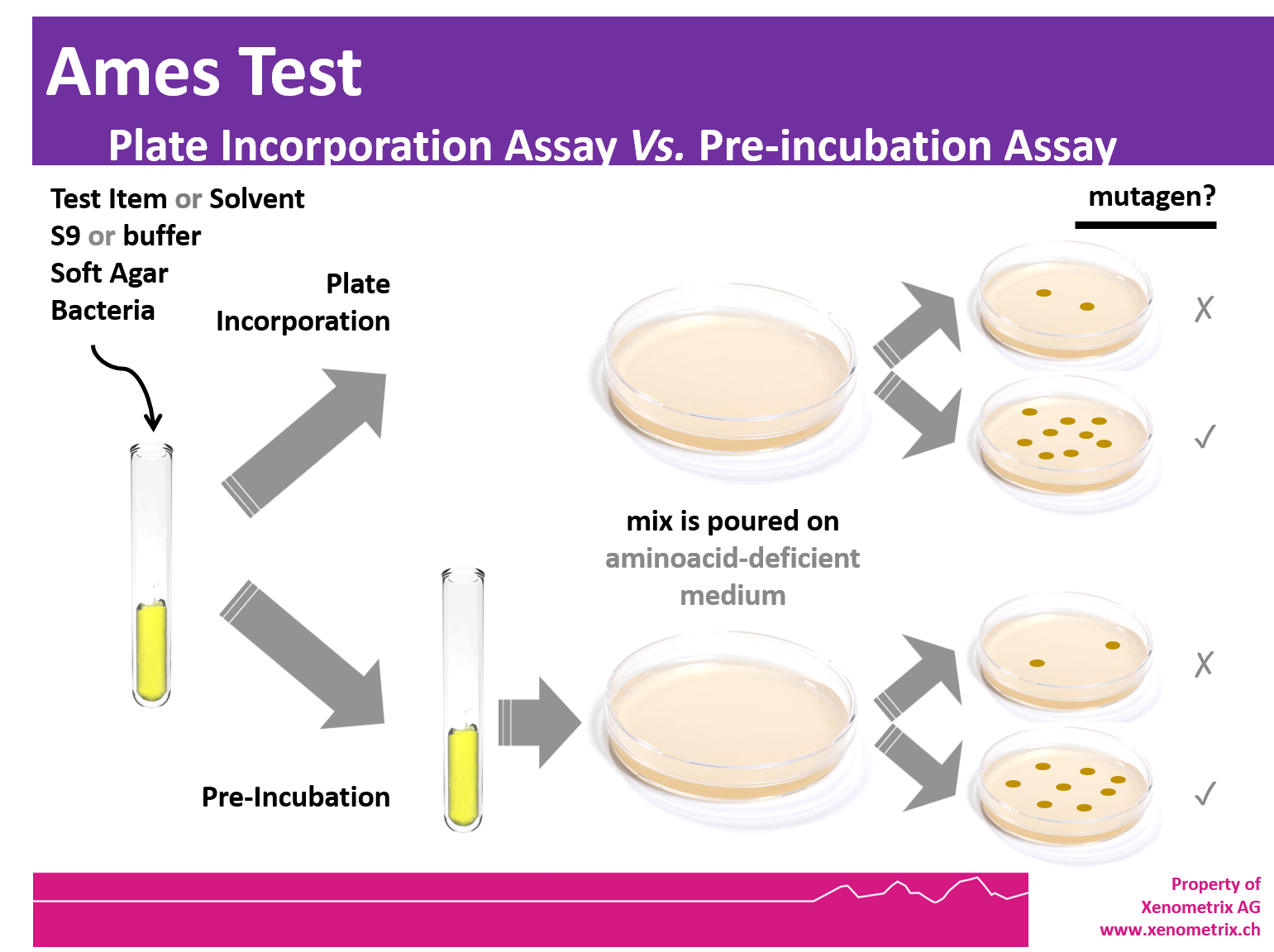
Le linee guida relative al test di Ames sono OECD 471, ICH M7.
Anche se fino a poco tempo fa l’Ames test su piastra è stato considerato il test più sicuro e più comunemente usato al mondo, con l’enorme aumento del numero di sostanze che necessitano questo tipo di test, la sua applicazione ai fini di screening è diventata poco pratica per i seguenti motivi:
- troppo laboriosa
- richiede troppa sostanza posta sotto il test
- richiede troppo tempo.
L’Ames test è molto utilizzato in ambito biomedico e farmaceutico-industriale per:
- analisi ambientali.
- analisi sperimentali di nuove molecole.
- controllo delle sostanze chimiche utilizzate per produrre i farmaci i quali, non per caso, devono seguire obbligatoriamente il test di GENOTOSSICITA’ sui batteri (direttiva 67/548/CEE).
- analisi dei prodotti cosmetici.
- dispositivi medici.
Test di Ames miniaturizzato.
Diverse forme di Ames Test miniaturizzati
- Ames Test miniaturizzato “Ames MPF™ “ basato sulla tecnologia della micropiastra liquida – 55 mg di campione per 5 ceppi, +/- S9.
- Ames Test miniaturizzato “MicroAmes24” sulla base di una piastra di agar da 24 pozzetti – 30 mg di campione per 5 ceppi, +/- S9
- Ames Test Ultra-miniaturizzato “NanoAmes™” basato su piastre di agar da 25 pozzetti quadrati – 35 ug di campione per 5 ceppi, +/- S9
- Ames Test Ultra-miniaturizzato “NanoAmes™ MPF” basato sulla tecnologia della micropiastra liquida in produzione.
AMES TEST MPF (Liquid Microplate Fluctuation) OECD 471, ICH M7
Descrizione del test
La crescita durante la notte è identica alla procedura descritta in precedenza (Test di Ames su piastre di agar – Descrizione del test).
I batteri vengono esposti a 6 concentrazioni di un campione da testare, nonché un controllo positivo e uno negativo, per 90 minuti in un terreno contenente una quantità sufficiente di istidina (S. typhimurium) o triptofano (E. coli) per supportare circa due divisioni cellulari.
Dopo l’esposizione, le colture (controllo negativo, campioni e controlli positivi) vengono diluite in un terreno indicatore di pH privo di istidina o triptofano e aliquotate in 48 pozzetti di una piastra da 384 pozzetti.
Dopo due giorni, le cellule che hanno subito la reversione alla prototrofia degli amminoacidi cresceranno. Nei kit liquidi Ames II / Ames MPF, il metabolismo batterico riduce il pH del terreno, cambiando il colore dei pozzetti in cui si trovano i batteri. Il numero di pozzetti contenenti colonie revertanti viene contato per ciascuna dose e confrontato con un solvente
(controllo negativo). Ogni dose viene testata in triplicato per consentire l’analisi statistica dei dati. Un aumento dose-dipendente e il significativo numero di colonie revertenti dopo l’esposizione del campione in esame rispetto ai controlli con solvente indica che il campione è mutageno.
Il potenziale mutageno dei campioni viene valutato direttamente e anche in presenza di attivazione metabolica, fornita da un omogenato di fegato, S9.
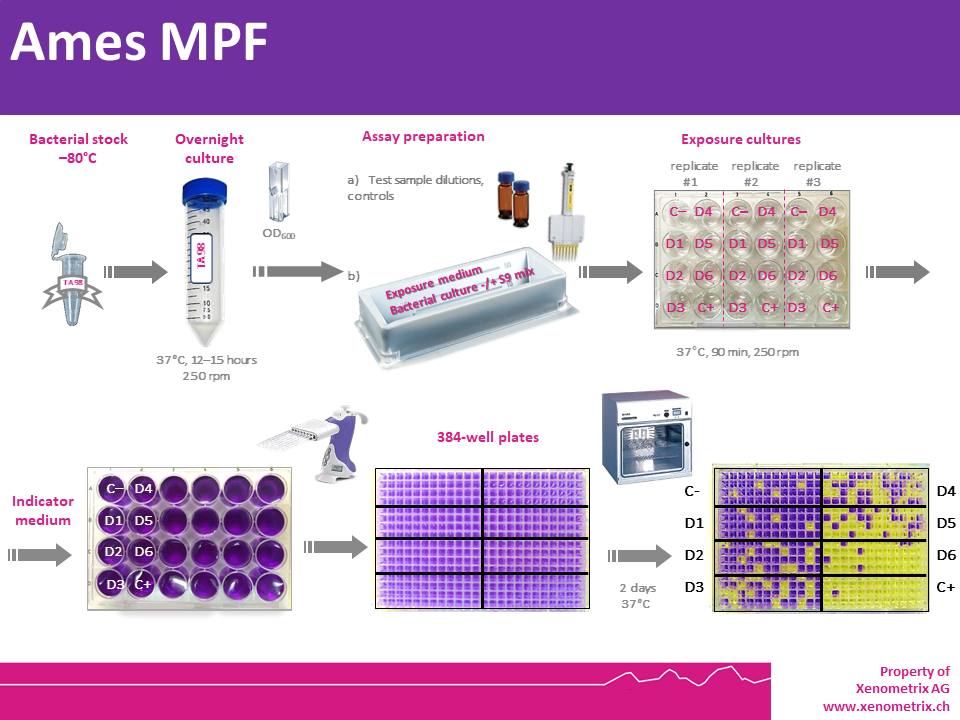
Le linee guida relative al test di Ames sono OECD 471*, ICH M7.
È una modifica del classico Ames test, in formato piastra microtiter che presenta una validissima alternativa, in quanto, pur rimanendo fedele ai principi di Ames test classico, offre numerosi vantaggi, quali:
- più veloce
- ceppi batterici controllati e con caratteristiche certe (nessuna necessità dell’analisi di
- genotipo)
- colorimetrico (più chiara interpretazione)
- in formato piastra microtiter (meno laborioso, più facile e pratico)
- più economico (richiede 6 volte meno la quantità della plasticheria)
La tecnica “end-point multiparametrica” diminuisce notevolmente sia il consumo del campione che la manualità stessa. Inoltre, elimina la potenziale variabilità fra i test eseguiti separatamente, causati dalla necessità di un maggior numero di passaggi.
I DIVERSI TIPI DI AMES TEST MPF MINIATURIZZATI – OECD 471 ICH M7
Ames MPF™ Penta 1
Cod. C01-512-S1-P – Cod.C10-512-S1-P – Cod. C01-512-S2-P – Cod. C10-512-S2-P
5 x 48/480 punti di misurazione: 1/10 campione in 5 ceppi (TA98, TA100, TA1535, TA1537,
E.coli uvrA/E.coli pkM101) se testato in 3 replicati, 6 diluizioni, +/- fegato di ratto S9 aroclor
1254 o PB/ß-Naphtoflavone-indotto, Controlli negativi e positivi. Non inclusi nel kit: soluzioni
di cofattore S9, micropiastre
Ames MPF™ Penta 2
Cod. B01-512-S1-P – Cod.B10-512-S1-P – Cod. B01-512-S2-P – Cod. B10-512-S2-P
5 x 48/480 punti di misurazione: 1/10 campione in 5 ceppi (TA98, TA100, TA1535, TA1537,
E.coli WP2 uvrA[pKM101]) se testato in 3 replicati, 6 diluizioni, +/- fegato di ratto S9 aroclor
1254 o PB/ß-Naphtoflavone-indotto, Controlli negativi e positivi. Non inclusi nel kit: soluzioni
di cofattore S9, micropiastre.
Per lo screening – ICH M7
Ames MPF™ 98/100
Cod. A01-210-S1-P – Cod.A10-210-S1-P – Cod. A01-210-S2-P – Cod.A10-210-S2-P
1/10 campione in 2 ceppi (TA98, TA100), se testato in 3 replicati, 6 diluizioni, +/- fegato di
ratto S9 aroclor 1254 o PB/ß-Naphtoflavone-indotto, Controlli negativi e positivi. Non inclusi
nel kit: soluzioni di cofattore S9, micropiastre.
Nei prossimi numeri descriveremo gli altre forme di test di Ames miniaturizzati.
Leggenda:
*IL FEGATO DI RATTO S9
enzima epatico mima il metabolismo dei mammiferi e attiva metabilicamente i mutageni. E’ utile quando ci troviamo davanti a sostanze che devono essere metabolizzate per vedere realmente se sono mutagene
** OECD 471 ed AMES MPF:
Almeno 5 Ceppi Batterici:
TA98 +/- S9, TA100 +/- S9, TA1537 or TA97 or TA97a +/- S9, TA1535 +/- S9, TA102 o E.coli wp2…. +/- S9
Metodi richiesti:
Plate incorporation method, Preincubation method, Fluctuation method, Suspension method
Quantità e Controlli richiesti: Quantità di composto raccomandata: 5mg/piastra o 5Ul/piastra; Attivazione metabolica raccomandata: +/- S9-medium; Triplicato; Controlli negativo e positivo; 5 dilutioni.